از همه چیز و همه جا
ما قصد داریم در این وبلاگ مطالب جالب همه رشته ها را قرار دهیم تا شما نیز از آن لظّت ببرید.
- ۲۳ شهریور ۹۴ , ۱۴:۱۰حدیثی از حضرت جواد الائمه(ع)
- ۲۳ شهریور ۹۴ , ۱۴:۰۵تسلیت شهادت حضرت جواد الائمه(ع)
- ۲۸ تیر ۹۴ , ۱۸:۴۴اظهار تأسف
- ۲۶ بهمن ۹۳ , ۲۰:۳۸دعوت مجدد
- مرداد ۱۳۹۹ (۱)
- مرداد ۱۳۹۷ (۱)
- بهمن ۱۳۹۶ (۱۰)
- اسفند ۱۳۹۵ (۴)
- شهریور ۱۳۹۵ (۱۰)
- تیر ۱۳۹۵ (۱)
- خرداد ۱۳۹۵ (۹)
- فروردين ۱۳۹۵ (۶)
- اسفند ۱۳۹۴ (۳)
- بهمن ۱۳۹۴ (۴)
- دی ۱۳۹۴ (۸)
- آذر ۱۳۹۴ (۲۰)
- مهر ۱۳۹۴ (۱۰)
- شهریور ۱۳۹۴ (۳)
- مرداد ۱۳۹۴ (۵)
- تیر ۱۳۹۴ (۱۲)
- خرداد ۱۳۹۴ (۳)
- ارديبهشت ۱۳۹۴ (۲۶)
- فروردين ۱۳۹۴ (۱۶)
- اسفند ۱۳۹۳ (۵)
- بهمن ۱۳۹۳ (۲۰)
- دی ۱۳۹۳ (۳۴)
- آذر ۱۳۹۳ (۲۷)
- آبان ۱۳۹۳ (۷)
- تیر ۱۳۹۳ (۱۰)
- ۹۹/۰۵/۲۹اعلام رسمی کوچ!!!
- ۹۷/۰۵/۰۴توصیه ی استاد حسن زاده ی آملی
- ۹۶/۱۱/۰۹شهید سید مرتضی آوینی
- ۹۶/۱۱/۰۹عمل کن
- ۹۶/۱۱/۰۹عزت یعنی...
- ۹۶/۱۱/۰۹خدا جون ممنون بابت برف
- ۹۶/۱۱/۰۹ما اهل کوفه نیستیم علی تنها بماند...
- ۹۶/۱۱/۰۹تفاوت را با برف احساس کنید
- ۹۶/۱۱/۰۹شهید حاج محمّد ابراهیم همت
- ۹۶/۱۱/۰۹بچّه بسیجی ها هواسشون باشه
-
فرهنگی
(۴۴) -
علمی
(۲۴) -
اسلحه
(۷) -
زیست محیطی
(۴) -
جالب و کاربردی
(۲۰) -
تکنولوژی
(۶) -
سرگرمی
(۷) -
هواپیما
(۳) -
سیاسی
(۳) -
درسی
(۹)
- ۹۴/۰۵/۲۱چگونه جدول تناوبی را حفظ کنیم
- ۹۳/۰۴/۲۸پوشش جانوری استان یزد
- ۹۴/۰۹/۰۲نمونه سوالات علمی مقایسه ای یزد
- ۹۴/۰۹/۲۲ak-47
- ۹۳/۰۸/۲۲عکس هایی از اسلحه های مدرن
- ۹۳/۰۴/۲۸بزرگترین اسلحه ی دنیا
- ۹۳/۰۴/۲۸اسلحه ی ژ3
- ۹۳/۰۴/۲۸اسلحه ی AK200
جفت مزدوج به اسیدها و بازهایی با ویژگی های مشترک گفته می شود. این ویژگی هایی مشترک،
در واکنش اسید و باز، یک اسید به یک باز اضافه می شود و واکنش آن ها یک باز مزدوج به اضافه ی یک اسید مزدوج تولید می کند.

مثال:
وقتی کلرید هیدروژن در آب حل می شود، تقریباً 100% آن با آب واکنش نشان می دهد تا یون های هیدرونیوم و کلرید تولید کند. کلرید هیدروژن یک اسید قوی است و ما در این جا می خواهیم این واکنش را به صورت یک طرفه بنویسیم:
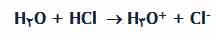
در واقع واکنش بین HCl و آب برگشت پذیر است اما تنها به مقدار بسیار کم!
برای فهم بیشتر، تصور کنید اسید HA واکنش برگشت پذیری در آب دارد:
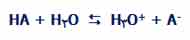
در واکنش رفت:
- • HA اسید است زیرا یک پروتون (یون هیدروژن) به آب می دهد.
- • آب باز است زیرا یک پروتون از HA می پذیرد.
در واکنش برگشت
- • +H3O اسید است زیرا یک پروتون (یون هیدروژن) به یون -A می دهد.
- • یون -A باز است زیرا یک پروتون از +H3O می پذیرد.
واکنش برگشت پذیر شامل دو اسید و دو باز است؛ ما به این جفت ها، جفت های مزدوج می گوییم:

زمانی که اسید HA پروتون از دست می دهد، باز -A تشکیل می دهد و زمانی که باز -A دوباره پروتون می پذیرد، به طور قطعی اسید HA را دوباره تشکیل می دهد.
این دو اسید و باز، یک جفت مزدوج هستند.
اعضای یک جفت مزدوج از طریق حضور یا عدم حضور یون هیدروژن قابل انتقال با همدیگر فرق دارند.
اگر در مورد اسید HA صحبت می کنید، -A باز مزدوج آن است و بالعکس.
آب و یون هیدرونیوم نیز یک جفت مزدوج هستند. زمانی که آب به عنوان باز عمل می کند، یون هیدرونیوم اسید مزدوج آن است؛ زیرا یک یون هیدروژن اضافی دارد که می تواند دوباره آن را از دست بدهد.
مثالی دیگر از جفت های مزدوج:
واکنش بین آمونیاک و آب را در نظر بگیرید:
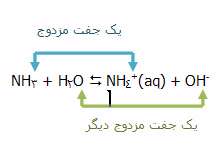
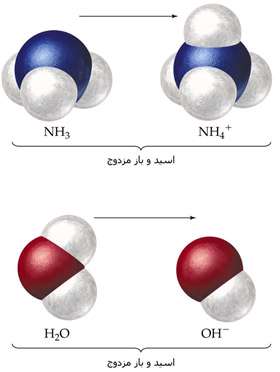
در واکنش رفت، آمونیاک باز است زیرا در حال گرفتن یون هیدروژن از آب است. یون آمونیوم نیز اسید مزدوج آن است چون می تواند یون هیدروژن را دوباره آزاد کند و آمونیاک تشکیل دهد.
آب به عنوان اسید عمل می کند و یون هیدروکسید، باز مزدوج آن است. یون هیدروکسید می تواند یک یون هیدروژن بگیرد تا آبرا دوباره تشکیل دهد.
توجه:
اسید یا باز قوی تر، مزدوج ضعیف تری دارد و اسید یا باز ضعیف تر، مزدوج قوی تری دارد.
در نهایت این که:

یافتن مزدوج جفت های اسید باز:
در هنگام یافتن اسید یا باز مزدوج به واکنش دهنده ها به دقت توجه کنید:
واکنش دهنده ای مانند یک اسید، متناظر با باز مزدوجی در سمت دیگر واکنش است.
برای شناسایی اسید مزدوج، به دنبال ترکیباتی که مرتبط با آن هستند، باشید. قبل و بعد از واکنش دادن را در نظر بگیرید؛
- منظور از قبل: سمت واکنش دهنده ها است و
- منظور از بعد: سمت محصولات است.
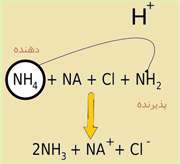
اسید مزدوج در سمت محصولات، یک یون هیدروژن به دست می آورد؛ بنابراین در سمت واکنش دهنده ها ترکیبی که یک یون هیدروژن کمتر از اسید مزدوج دارد، یک باز است.
باز مزدوجی که در سمت محصولات است، یک یون هیدروژن از دست داده و بنابراین در سمت واکنش دهنده های واکنش، ترکیبی که یک یون هیدروژن بیشتر از باز مزدوج سمت محصولات دارد، یک اسید است.
سؤال: با این سؤال اطلاعات خود را بسنجید.
در واکنش 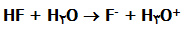 کدام اشتباه است؟
کدام اشتباه است؟
(الف) HF اسید است زیرا یک پروتون به H2O می دهد.
(ب) -F باز مزدوج است زیرا از آب یک پروتون گرفته است.
(ج) -F باز مزدوج است زیرا با اسید HF در یک پروتون فرق دارد.
(د) +H3O اسید مزدوج است زیرا با آب که باز است، در یک پروتون فرق دارند.
مرکز یادگیری سایت تبیان - تهیه: خدیجه آلچالانلو
تنظیم: یگانه داودی
بسم الله الرحمن الرحیم
پلیس خوب پلیس بد
کسانی که با بازی شطرنج آشنا هستند خوب می دانند در این بازی شما در واقع با خودتان بازی می کنید نه با حریف!
اجازه دهید توضیح بیشتری بدهم.
شما اول باید خودتان را جای حریف بگذارید و بگویید اگر من جای او می بودم و این داشته هایم بود (مهره ها) چنین حرکت هایی را ممکن بود انجام دهم .
و سپس نسبت به حدسی که در باره خودتان از زبان حریف زده اید واکنش نشان داده و با مهره های خودتان بازی می کنید.
داستان سیاست نیز همین است. علی الخصوص وقتی بازی شما میلیون ها بیننده هم دارد دیگر یک بازی تمرینی نیست بلکه شاید بازی کردن با احساسات و غرور و منافع ملی مردم سرزمینت باشد.
چند صباحی است که بحث مذاکره با امریکا بر سر زبان ها افتاده و دستگاه دیپلماسی کشور در سطح روسای جمهور و وزیران خارجه پس از 34 سال شاهد شکسته شدن قبح این مسئله در تاریخ دو کشور است.
طبیعی است که طرفین مذاکره به دنبال حد اکثر کردن سود خود در کنار حداقل امتیاز اعطایی به طرف مقابل هستند .
قطعا اساسی ترین عنصر در این میان داشته های طرفین یا همان "دست پر" است .
اما نباید فراموش کرد همچون بازی های ورزشی میزبان بودن در یک بازی، خود یکی از عناصر اصلی برد محسوب می شود. (اسمش را بگذارید جنگ روانی طرفین)

پس از آغاز مذاکره طرف امریکایی سریعا جبهه خود را چید و در این میان دستگاه اجرایی امریکا خواهان مذاکره (پلیس خوب) و کنگره امریکا خواهان افزایش تحریم ها شد (پلیس بد).
در چنین شرایطی قدرت چانه زنی پلیس خوب افزایش می یابد و به طرف مقابل می فهماند فرصت با من بودن را قدر بدان وگرنه با او (پلیس بد یعنی کنگره) طرفی !
آیا به نظر شما در این سوی میز مذاکره نیز نیازی به داشتن پلیس بد نداریم ؟
قطعا عقل ایجاب می کند چنین باشد.
اگر امریکایی ها به این نتیجه برسند که مثلا عموم مردم ایران خواهان ارتباط هستند شک نکنید مذاکره کننده های ما شرایط بسیار سختی خواهند داشت.
امریکایی ها تمام مخالفت های مردمی و سیاسی نسبت به مذاکره را رصد می کنند. و هرچه مخالفت های داخلی بیشتر باشد قدرت چانه زنی طرف ایرانی هم بیشتر خواهد بود .
متاسفانه عده ای نادان در چنین شرایطی دائم بر طبل اثر تحریم ها بر ایران در داخل می کوبیدند و دقیقا اسرائیل هم با همان صدای طبل می رقصید.
دوستان و عزیزان ما همه باید به دولت جدید در گرفتن امتیاز های بیشتر کمک کنیم و به انتخاب مردم کشورمان احترام بگذاریم ما باید به دید اعتماد به دولت خود و بی اعتمادی به امریکایی ها به جریان نگاه کنیم.
به سخن رهبری پس از تحرکات دیپلماسی در نیویورک دقت فرمایید:
«ما از تحرک دیپلماسی دولت از جمله سفر نیویورک حمایت میکنیم زیرا به دولت خدمتگزار اعتماد داریم و به آن خوشبین هستیم اما برخی از آنچه که در سفر نیویورک پیش آمد بجا نبود، چون ما دولت آمریکا را غیرقابل اعتماد، خودبرتربین، غیرمنطقی و عهد شکن میدانیم.»
خوب اگر نگاه کنید در این چند جمله کوتاه تمام عناصر سیاسی و عملیات روانی مدنظر رعایت شده است.
قطعا راهپیمایی سیزده آبان امسال باید پرشور تر و با شعار های کوبنده تر بر گزار شود تا امریکایی ها بفهمند آنچه امروز پیش آمده یک فرصت برای آنهاست و قرار نیست باب مذاکره همیشه باز باشد و شک نکنید این عینا خواسته دستگاه دیپلماسی ماست.
امریکایی ها امروز برای حل مشکلاتشان در منطقه نیاز جدی به تدابیر ایران دارند.
و این مدیون مقاومت مردم ایران است که قدرت چانه زنی ما را بالا برده است.
حضور جدی در سوریه، عراق ،فلسطین و لبنان و ایجاد یک وزنه نظامی چشمگیر توسط ایران و از طرفی دیگر رسیدن به مرز 17000 سانتریوفیوژ شرایط را دگرگون کرده است.
ایران ، ایران سال های 2006 نیست. و این را خوب امریکایی ها می فهمند آنها معنی مشارکت 75 درصدی را هم متوجه هستند.
لذا از سر دادن فریاد مرگ بر امریکا هراسی نداشته باشید که این بار علاوه بر اجر معنوی اجر دنیوی هم دارد.
بسم الله الرحمن الرحیم
چند تن از دوستان و نزدیکان طی تماس های تلفنی اعلام کردند که به نقل از بنده پیامکی با این مضمون در حال انتشار است:
محرمانه – فوری :
رائفی پور به یکی از دوستان گفته BBC با همکاری دولت و با واسطه ترکان در حال تهییه مستندی است که بگوید شهدای هسته ای جاسوسان امریکا و انگلیس بودند ایران آنها را کشت و...!!
در پاسخ به این افراد باید گفت:
"این القاطع حبائل الکذب و الافترا"
اما تحلیل بنده در باره این شایعه:
این ماجرا از 4 حالت احتمال ریاضی خارج نیست:
الف: رائفی این سخن را گفته است اما صحت ندارد:
در این صورت رائفی باید پاسخ گوی این مطلب باشد که با چه نیتی چنین حرفی را زده است.
ب:رائفی این سخن را نگفته و صحت هم ندارد:
در این صورت این مطلب صرفا یک شایعه بی اساس است و دقیقا مثل این است که از قول بنده بگویند ساکنان مریخ سه چشم دارند ، به قول معروف شنونده باید عاقل باشد.
ج: رائفی این سخن را گفته و صحت هم دارد :
در این صورت باید از رائفی خواست اسنادش را اعلام کند چرا که این ماجرا خیانت آشکار به خون شهداست و قطعا باید آبروی این افراد را در پیش گاه مردم برد.
د: رائفی این سخن را نگفته اما آنچه به اسم او نقل شده صحت دارد:
در این صورت طراحان این پروژه با استفاده از محبوبیت رائفی در میان مخاطبان خاصی که او دارد در حال انتشار خبر مهمی هستند که صرف نظر از اینکه چه کسی آن را نقل کرده آن خبر اهمیت فراوانی دارد و در واقع عبارت " قال رائفی " ابتدای آن با قید "محرمانه و فوری" سبب سرعت انتشار آن می گردد.
مثل اینکه چند روز پیش یکی از دوستان به بنده فرمودند مقاله ای تهییه کرده اند در باره یکی از موضوعات قرانی و خواستند به نام بنده منتشر شود تا چون "قال رائفی " دارد بیشتر مد نظر قرار گیرد.
به هر حال رائفی اگر حرفی داشته باشد در همین وبلاگ می زند و از احدی هم واهمه ای ندارد.
این که در این پیامک آمده : "رائفی پور به یکی از دوستان گفته" عموم عناصر خبری آن مبهم است و ارزش خبری ندارد
احتمالا این هم پروژه عملیات روانی جدید علیه بنده است تا موجب بوجود آمدن حساسیت دولت بر روی بنده شود ...
و الله اعلم بما فی صدورهم...
به امید ظهور مولی و سرورمان حضرت حجت (عج) که صد البته نزدیک است...
به نقل از :http://antisemitism.blogfa.com
فرایند سل-ژل (به انگلیسی: Sol-gel) که همچنین با نام رسوبدهی محلول شیمیایی (به انگلیسی: Chemical Solution Deposition) از آن یاد میشود، یک روش شیمی تر است که درمهندسی و علم مواد و مهندسی سرامیک به طور گسترده استفاده میشود. این روش معمولاً برای تولید مواد (به عنوان مثال اکسید فلزات) با شروع از یک محلول کلوئیدی(سل) که به عنوان پیشماده برای یک شبکه بههمپیوسته (ژل) از ذرات گسسته یا پلیمرهای شبکهای است، بکار میرود. پیشمادههای معمول شامل آلکوکسید و نمک فلزات (از قبیل کلریدها، نیتریدها و استاتها)هستند که تحت واکنشهای مختلف هیدرولیز و بسپارش مرحلهای قرار میگیرند.
انواع روش های سل- ژل بر اساس نوع پیش ماده مورده استفاده
تقسیم بندی بر اساس نوع نمک
۱-پیش ماده های آلکوکسیدی
۲-پیش ماده های نمک فلزی
تقسیم بندی بر اساس نوع محیط پیرامون
۱-پیش ماده های پلیمری
۲-پیش ماده های آبی
کلوئید
اصطلاح کلوئید از ترکیب دو کلمه یونانی Kolla (به معنی چسب)و eidos (به معنای شبیه)بدست آمده است که اولین بار توسط دانشمند انگلیسی بنام توماس گراهام بکار برده شد.
سل
عموماً سل عبارت است از سوسپانسیون پایدار از ذرات جامد کلوئیدی و یا پلیمری که در یک مایع قرار دارند . این ذرات می توانند آمورف و یا کریستالی باشند . ذرات جامد کلوئیدی که ابعادی نانومتری دارند از طریق دو واکنش تشکیل می شوند به زبانی سادهتر سل مخلوطی است از جامدهایی با اندازههای متفاوت و بین 1 تا 100 نانومتر در آب که ته نشین نمیشوند و عبارتند از:
۱) هیدرولیز: در اثر حل شدن نمک در آب، کاتیون فلزی با آب کمپلکس تشکیل می دهد . در این حالت انتقال جفت الکترون از مولکول آب به اربیتال های خالی کاتیون فلز واسطه وجود دارد . بار جزئی هیدروژن افزایش می یابد و مولکول آب خاصیت اسیدی پیدا می کند . بر اساس مقدار اسیدی بودن آب ، انواع واکنش های هیدرولیز را می توان د اشت. به طور کلی با افزایش دانسیته بار فلز، افزایش تعداد پل های یون های فلزی توسط لیگاند های اکسو و هیدروکسو و افزایش تعداد هیدروژن موجود در لیگاندها، هیدرولیز آسان تر می شود .
۲) کندانسیون: این واکنش توسط دو مکانیزم مختلف هسته دوستی انجام می شود و بستگی به عدد همسایگی فلز دارد . وقتی عدد همسایگی مورد نظر مهیا باشد، کندانسیون توسط یکواکنش جانشینی هسته دوستی انجام می شود و وقتی عدد همسایگی مورد نظر فلز مهیا نباشد، افزودنی هسته دوستی وجود دارد. واکنش کندانسیون که در واقع نوعی پلیمراسیون محسوب می شود خود به دو دسته تقسیم می شود:
۱- الیشن: یک فرایند کندانسیون است به طوری که پل های هیدروکسیدی بین دو فلز به وجود می آید.
۲- اکسیلیشن: واکنش کندانسیونی است که در آن پل های اکسیژنی بین دو فلز به وجود می آید .
مراحل تشکیل سل
مراحل تشکیل سل به طور کلی به دو دسته تقسیم بندی می شوند:
۱- تشکیل محلولی حقیقی از پیش ماده ها(پیش ماده های آلکوکسیدی یا پیش ماده های نمک فلزی) مورد نظر در حلال که می تواند آب، الکل یا اسید باشد.
۲- تشکیل محلول کلوئیدی(سل) از طریق تبدیل اتم های فلزی به کامپلکس های فلزی توسط واکنش های هیدرولیز و کندانسیون، که در واقع واکنش های به وجود آورنده ذرات کلوئیدی می باشند، با انجام این واکنش ها ذرات بزرگ شده و به ابعاد ذرات کلوئیدی یعنی ۱nm تا حدود ۱۰۰nm می رسند. در این مرحله نانوذرات که معمولاً آمورف می باشند تشکیل شده است.
۳- پایدار کردن ذرات کلوئیدی و جلوگیری از ته نشین شدن آن ها توسط یک عامل پایدار کننده. این عامل می تواند توسط کنترل عوامل محیطی از قبیل کنترل pH، دمای سل، میزان همزدن سل کنترل شود یا از طریق افزودن مواد شیمیایی کنترل گردد.
تفاوت سل با محلول
کلوئیدها از یک نظر شبیه محلولها هستند و از جهاتی دیگر بکلی با آنها متفاوتند. هر سیستم کلوئیدی حداقل دارای دو بخش است:
۱ – فاز پراکنده
۲ – محیط پراکندگی
اما محلولهای حقیقی فقط یک فاز دارند و ماده حل شده و حلال باهم یک فاز را تشکیل میدهند. تفاوت بعدی اندازه ذرات در سل یعنی کلوئیدها و اندازه ذره در محلول یعنی اتم ها و یون ها است. در سل اندازه ذرات کلوئیدی معمولاً بین ۵۰ تا ۲۰۰۰ آنگستروم است. اما در محلول اندازه اتم ها و یون ها در حد آنگستروم است.
اندازههای کلوییدی
اگر جسمی را که نرم ساییده شده است در آب بریزیم، یکی از سه حالت زیر پیش میآید:
۱. ممکن است یک «محلول حقیقی» تشکیل شود که نتیجهی پراکنده شدنِ اتمها، مولکولها یا یونهای آن جسم در یک حلاّل است. اندازهی ذرات در این محلول از حدود ۱nm تجاوز نمیکند؛
۲. این امکان وجود دارد که ذراتِ بزرگتر از حدود ۱۰۰nm باقی بمانند. این ذرات میکروسکوپی، بهتدریج تهنشین میشوند. از آنجا که این ذرات به طور موقت معلقاند و بر اثر ماندن تهنشین میشوند، به مخلوط حاصل، «مخلوط معلق» یا «سوسپانسیون» میگویند؛
۳. ذراتی که اندازهی آنها از ۱nm تا حدود ۱۰۰nm تغییر میکند، معمولاً به صورت پراکنده در همهجای محیط باقی میمانند. این نوع مخلوط «کلویید» نامیده میشود. به عبارت دیگر، در یک مخلوط کلوییدی با «نانوذرات» سروکار داریم.
کلوییدها در میانهی سوسپانسیونها و محلولها قرار میگیرند، ولی ناهمگن به شمار میروند. محیطهای پیوسته همچون آب یا الکل و جسم پراکنده، هرکدام وضعیت جداگانهای به وجود میآورند.
پایدار سازی سل
منظور از پایدار سازی سل این است که ذرات کلوئیدی ته نشین نشوند و همچنان به صورت سوسپانسیون باقی بمانند تا بتوان همچنان به آن طبق تعریف سل گفته شود.پایداری و یا انعقاد سل در فرایند سل - ژل بسیار مهم می باشد و ساختار و شبکه ژل به دست آمده با اندازه و شکل ذرات تجمع یافته اولیه مرتبط می باشد .
انواع سل
سل کلوئیدی
منظور از سل کلوئیدی سلی است که در آن تشکیل ژل فقط از طریق چسبیدن(آگلومراسیون) ذرات کلوئیدی بوجود می آید.
سل های کلوئیدی مونودیسپرس
در این نوع سل ها، تمام ذرات دارای شکل و اندازه یکسان می باشند و تشکیل این نوع سل به دلیل میل شدید به آگلومره شدن بسیار دشوار است.
سل های کلوئیدی پلی دیسپرس
اکثر سیستم های کلو ئیدی به این صورت می باشند و اندازه ذرات در آنها یکسان نیست و برای بیان اندازه ذرات از متوسط مقادیر استفاده می شود.
سل های ماکرومولکولی یا پلیمری
منظور از سل پلیمری سلی است که در آن تشکیل ژل از طریق اتصال ذرات کلوئیدی توسط زنجیره های پلیمری بوجود می آید. در این سیستم ها رشد ذرات با تشکیل پلیمر صورت می گیرد و اینپلیمرها با یکدیگر اتصال برقرار کرده و سپس حلال ر ا در میان خود به تله می اندازند و سرانجام یک جسم نیمه جامد تشکیل می شود که به آن ژل می گویند. این نوع سل ها معمولاً از ارگانومتالیک های محلول در الکل حاصل می شوند.
مکانیزم پایدار سازی در سل های کلوئیدی
پایداری یک سل کلوئیدی بستگی به مقدار پتانسیل زتا دارد، به طوری که هرچه پتا نسیل زتا بیشتر باشد پایداری سل بیشتر می باشد . برای یک پتانسیل سطحی یکسان، سد و نیروی دفعی برای ذرات بزرگتر بیشتر می باشد . ارتباط متفاوت بین نیروی جاذبه و نیروی دافعه با اندازه، سبب می شود که وقتی اندازه ذرات از حدی بزرگتر شد، نیروی دافعه بر نیروی جاذبه غلبه کرده و سل پایدار شود.
موارد متاثر در انعقاد(آگلومره شدن و تشکیل ژل) در سل های کلوئیدی
اصولاً انعقاد ذرات سل ناشی از موارد زیر می باشد:
۱- کاهش پتانسیل سطحی ناشی از تغییردر pH پی اچ
۲- افزایش غلظت الکترولیت در حلال.
پپتیده شدن
در بعضی مواقع کلوئید انعقاد یافته، می تواند دوباره پخش شود که به این فرایند پپتیده شدن گفته می شود.
مکانیزم تشکیل نانوذرات در سل های کلوئیدی
سه نوع مکانیزم مختلف برای تشکیل نانو ذرات و جلوگیری از درشت شدن ذرات در سل های کلوئیدی پیشنهاد شده است که عبارتند از:
مکانیزم دافعه الکترواستاتیک[ویرایش]
مکانیزم دافعه فضایی
مکانیزم دافعه الکترواستاتیک و فضایی به صورت همزمان
مکانیزم پایدار سازی در سل های پلیمری
مکانیزم پایدار سازی در سل های پلیمری عبارتست از تشکیل یک ابر مولکول که همچون یک نخ تسبیح طویل که مهره های آن در واقع همان ذرات کلوئیدی می باشنددر سزتاسر ظرف واکنش گسترش میابد و بدین ترتیب با فراهم آوردن بستری مناسب باعث جلوکیری از رسوب ذرات کلوئیدی می گردد. در واقع این روش را می توان به درخت سیبی تشبیه کرد که در آن شاخه های اصلی و فرعی درخت همان شبکه پلیمری و میوه ها ذرات کلوئیدی می باشند که بعد از کلسیناسیون به فرم نانو ذره تبدیل می شوند.
مکانیزم تشکیل نانو ذرات در سل های پلیمری
مکانیزم تشکیل نانو ذرات در سل های پلیمری یا ماکرومولکولی هر عاملی است که موجب پایداری شبکه پلیمری یا ابر مولکولی بوجود آمده می شود. در واقع هر عاملی که بتواند مانع از کراس لینک شدن پلیمر شود و یا هر عاملی که موجب تشویق فرایند پلیمراسیون گردد. این ابر مولکول حاصل واکنش شیمیایی فیمابین مواد مورد استفاده جهت تشکیل یک پلیمر می باشد. به عنوان مثال در روش پچینی این ابر مولکول حاصل بسپارش مونومر استر می باشد که حاصل از واکنش استری شدن بین اسید سیتریک و اتیلن گلیکول می باشد. هر عاملی که موجب کراس لینک شدن این ابر مولکول شود برای تشکیل نانو ذرات مضر می باشد.
ژل
عبارت است از یک شبکه پیوسته سه بعدی متخلخل که یک فاز مایع را در خود جای داده است. دراکثر سیستم های سل - ژل، تشکیل ژل با ایجاد پیوندهای کووالانسی بوده و ژل برگشت پذیر نیست یعنی قابلیت برگشت به حالت سل را ندارد. اگر ژل حاصل دارای پیوندهای دیگری غیر از پیوند کووالانسی باشد می تواند برگشت پذیر باشد.
انواع ژل بر اساس مکانیزم تشکیل
ژل های کلوئیدی
در ژل کلوئیدی، شبکه توسط آگلومره شدن(چسبیدن) ذرات کلوئیدی به وجود می آید.
ژل پلیمری
در ژل پلیمری شبکه دارای یک ریز ساختار پلیمری می باشد به عبارتی واحدهای پلیمری می باشند که تشکیل ژل می دهند.
مراحل تشکیل ژل
بعد از مراحل ۳ گانه که در تشکیل سل بیان شد، مراحل تشکیل ژل که در واقع در دنباله مراحل تشکیل سل است بسته به نوع ژل(کلوئیدی یا پلیمری) عبارتند از:
۱- اگر ژل کلوئیدی باشد، از به هم چسبیدن ذرات کلوئیدی توسط نیروهای ضعیف واندروالسی در اثر تبخیر حلال پیرامون ذرات کلوئیدی بوجود می آید.
۲- اگر ژل پلیمری باشد، یعنی محیط پیرامون ذرات کلوئیدی از مولکول هایی تشکیل شده باشد که مستعد تشکیل یک زمینه پلیمری باشد، در این صورت ذرات کلوئیدی همانند کشمش در یک کیک کشمشی تثبیت می شوند، لذا با تغییر عوامل پیرامونی مثل تنظیم pH، دما و زمان و یا افزودن مواد شیمیایی می توان به پایدار سازی این شبکه پلیمری سوق پیدا کنیم. سپس با قرار دادن این ژل تشکیل شده در داخل آون می توان از شر شبکه پلیمری پیرامون آن خلاصی پیدا کرد و فقط نانو ذرات را خواهیم داشت. در نهایت با قرار دادن محصول حاصل در کوره با دانستن کمترین دمای کلسیناسیون می توان نانوذرات آمورف را به نانو ذرات کریستالین تبدیل نمود.
انواع ژل بر اساس طرز خشک شدن
زیروژل(Xerogel)
خروج حلال از حفرات در هنگام خشک کردن باعث ایجاد نیروی مویینگی شده و در نتیجه سبب انقباض شبکه ژل می شود . ژلی که در اثر خشک شدن به دست می آید زیروژل نامیده می شود. زیروژل نسبت به ژل تر اولیه معمولاً حجم کمتری دارد و به علت استرس ناشی از خشک کردن ، ژل یکپارچه خراب شده و پودر حاصل می شود .
ایروژل(aerogel)
وقتی که ژل تر تحت شرایطی خشک شود که شبکه و حفرات تغییر حجم نداده و در نتیجه حجم ژل خشک به دست آمده برابر با حجم ژل تر باشد،این ژل چون درآن انقباض رخ نداده، که به این ژل حاصل شده ایروژل گفته می شود. بسیار دانسیته کمی دارد و شدیداً متخلخل می باشد ولی در آن استرس های ناشی از انقباض وجود ندارد. اگر ژل خیس درون اتوکلاو قرار داده شود و تحت شرایط خاصی خشک شود، ممکن است میزان انقباض به دلیل حذف فشار موئینگی اندک باشد. این فرایند به خشک کردن بحرانی موسوم است و محصول حاصل نیز ایروژل نامیده می شود.
انواع ژل بر اساس نوع حلال
آلکوژل(Alchogel)
ژلی است که نوع حلال آن یک الکل بوده است.
هیدروژل(Hydrogel)
ژلی است که حلال آن آب بوده است.
منبع:ویکی پدیا
لیگاند
لیگاند (به انگلیسی: Ligand) در شیمی به مولکول یا یونی گفته میشود که با فلز مرکزی پیوند برقرار کرده و ترکیب کمپلکس دهد.
سایتهای فعال در لیگاند
تعداد سایتهای فعال در لیگاندها متغیر است. در شیمی معدنی لیگاند دارای چند سایت فعال برای حمله به یک فلز را لیگاند کیلات کننده مینامند.
در شیمی آلی فلزی لیگاندهای دو یا چند دندانه به سه شکل دانگل، کی لیت و یا پل به فلز متصل می شوند.
قدرت لیگاند
قدرت لیگاندهای مختلف در تشکیل پیوند با فلزات با هم تفاوت دارد. تفاوت قدرت لیگاندها باعث تفاوت در مقدار شکافتگی سطوح انرژی در فلز در اثر حضور لیگاند میشود. این مورد از مباحث نظریه میدان لیگاند است.
اثر قدرت لیگاند در ساختار ترکیبات کمپلکس
به دلیل تفاوت مقدار میدان لیگاندها ساختمان ترکیبات کمپلکس از هم متفاوت است. این ترکیبات میتوانند ساختاری هشت وجهی یا چهاروجهی داشته باشند.
منبع:ویکی پدیا
محققان آمریکایی چسب جدیدی را معرفی کردهاند که هیچ کدام از مشکلات موجود در سرهم کردن اشیاء شکسته با چسبهای بسیار قوی مانند خشک شدن زودهنگام یا بسیار دیرموقع آنها را ندارد.
به گزارش ایسنا، چسب "باندیک" مایعی است که مانند یک دستگاه جوشکاری، اشیاء پلاستیکی را در عرض چهار ثانیه به هم میچسباند، اما محکم شدن چسب تنها با تاباندن نور فرابنفش روی محل چسبانده شده صورت میگیرد.
محتوای بستهبندی "باندیک" شامل دو پد تمیزکننده گرد و غبار، قلم باندیک و یک کارتریج چسب مایع است. باندیک این قابلیت را دارد که عملیات خشک شدن چسب در زمان دلخواه شما صورت بگیرد.
روش استفاده از این محصول بدین شکل است که ابتدا محل مورد نظر را با استفاده از پد ویژه باندیک از گرد و غبار تمیز کرده، سپس چراغ الایدی باندیک را فعال کرده و با استفاده از سر سوزنی شکل قلم باندیک نقطه مورد نظر را چسبکاری میکنیم. پس از این که تکههای جدا شده را به درستی در جای خود مستقر کردیم با چراغ باندیک نور فرابنفش را روی محل چسبانده شده میگیریم.
پس از چهار ثانیه چسب مایع به خوبی سفت شده و میتوانید شیئ آسیبدیده را مانند سابق مورد استفاده قرار دهید.
از این محصول برای چسباندن اشیایی از جنس چوب، فایبرگلاس، پلاستیک و آهن میتوان استفاده کرد. باندیک را میتوان برای پرکردن قسمتهای تحلیل رفته برخی اشیاء مانند کابلهای یو اس بی نیز استفاده کرد، بدین شکل که پس از چسبکاری قسمت مورد نظر را با استفاده از سوهان به شکل دلخواه درآورده، آن را رنگ کرده و واکس بزنیم.
بسته کامل باندیک را میتوان با قیمت 22 دلار آمریکا خریداری کرد. - See more at:
فیزیکدانانی از مرکز سینکروترونِ* SOLEIL در فرانسه با استفاده از شتاب دهنده ذرات توانستند بهترین موقعیت را برای درک آزمایش ذهنی که نخستین بار در سال ۱۹۲۷ توسط آلبرت اینشتین پیشنهاد شده بود، انجام دهند. به نظر می رسد اینشتین در جدال با بور شکست خورده است.

تصویری از شتاب دهنده ی ذرات SOLEIL در فرانسه
به گزارش انجمن فیزیک ایران، در نوعی از آزمایش بسیار محبوب دو شکافی، اندازهگیریها جنبهای از نظریهی کوانتومی که اینشتین در صدد نامعتبر کردنش بود را تائید میکنند. این آزمایش به جای دو شکافیِ آزمایش اینشتین، از دو اتم برانگیخته استفاده میکند و نشان میدهد که هرگاه بتوان تعیین کرد از کدام اتم یک الکترون تابش کرده است، طرح تداخلی کوانتومی ناپدید میشود. اینشتین چندین بار تلاش کرد تا عدم قطعیت ذاتی در مکانیک کوانتومی را با مطرح کردن آزمایشاتی فرضی که در آن زمان قابل انجام در آزمایشگاه نبودند، رد کند. یکی از آنها شامل اصل دوگانگی موج-ذره میشد که پیشبینی میکند دنبالهای از تک ذرات که از دو شکاف عبور می کنند، طرح پراشی موجگونه را روی پرده ایجاد خواهند کرد. این اثر به علت خاصیت موجگونهی هر ذره است که به آن اجازه میدهد همزمان از هر دو شکاف عبور کند.
اینشتین میگفت، یک حسگر فوق العاده حساس میتواند اثرات شکافی که الکترون از آن عبور کرده را بدون اینکه طرح تداخلی را برهم بزند آشکار کند. این به نوعی ایستادن در برابر مکانیک کوانتومی بود و رقیب بزرگ اینشتین، نیلز بور، با این بحث که اگر آزمایشگر بداند الکترون از کدام شکاف گذشته است اصلاً طرح تداخلی رخ نخواهد داد و با آن مخالفت میکرد.
در حالی که آزمایش مذکور در آن زمان بدلیل ساده بودن مفهوم و در عین حال دشواری تجربیاش کاملاً فرضی بود، همین نکات آزمایشگران امروزی را به طرز مقاومت ناپذیری به چالش کشیده است. در سال ۲۰۰۱، سرگ هاروچ (Serge Haroche) و همکارانش در پاریس این اصل را نشان دادند. آنها برای شکافتن حالت داخلی تعدادی اتم ریدبرگ به دو حالت مختلف که قبل از باز ترکیب شدن با آهنگهای متفاوتی ظاهر میشدند، از پالس مایکروویو استفاده کردند. بعد از آن در ۲۰۱۱، جورج اشمیدمایر Jorge Schmiedmayer و همکارانش در دانشگاه صنعتی وین به تقریب نزدیکتری دست یافتند.
آزمایش دو-اتمی
اکنون، کاتالین میرن و همکارانش در شتاب دهنده ذرات SOLEIL با همراهانی از سوئد، فرانسه و رومانی به بازآفرینی آزمایش فرضی اصلی بسیار نزدیک شدهاند. آنها از یک مولکول دو اتمی اکسیژن که توسط تابش سینکروترونی و قابل تنظیمِ پرتوی X در خط باریکهی PLÉIADES برانگیخته شده است، استفاده میکنند. با تنظیم انرژی پرتوی X، محققان میتوانند یک الکترون را تحریک کنند تا از مدار مولکولی داخلی به یک حالت مقید با انرژی زیاد یا به یک حالت دفعی که منجر به واپاشی مولکول میشود برود. بعد از این گذار، یکی از اتمها، الکترون دیگری به نام الکترونِ آگر (Auger electron) تابش کرده و در این حین پس زده میشود. اگر الکترون اول به حالت مقید رفته باشد، دوباره به حالت پایهی مولکولی برمیگردد و موقع رها شدن الکترون آگر، دو اتم با هم پس زده میشوند.
این یعنی اندازهگیری پس زنیِ اتمها هیچ چیز در مورد اینکه کدام اتم الکترون را تابش کرده است نمیگوید. اما اگر الکترون به حالت دفعی رفته باشد، مولکول واپاشی می کند و دو تک اتم اکسیژن ایجاد میکند. چناچه الکترون آگر بعد از واپاشی مولکول آزاد شود، اتمها دیگر با هم پس زده نمیشوند و اندازهگیری پس زنی اتمها مشخص خواهد کرد که الکترون از کدام اتم تابش شده است. لذا، این دو اتم نقش شکافهای آزمایش فرضی را بازی میکنند و آزاد شدن الکترون مانند بیرون آمدن ذره از دو شکافی است. اگر پس زنی اتم ها با هم باشد، نمیدانیم الکترون از کدام شکاف گذشته است- اما اگر فقط یکی پس زده شود، آنگاه می دانیم کدام شکاف مورد استفاده قرار گرفته است.
به جای پرده، تیم تحقیقاتی از دستگاه دست ساز منحصر به فرد و بسیار حساسی به نام EPICEA استفاده کرد که هر سه مولفهی تکانه را هم در الکترون تابش شده و هم در اتم پس زده شدهی اندازه می گرفت. میرن میگوید: «این در واقع چیزی بود که من برای رساله دکترای خودم بیست سال پیش ساختم».
اینشتین باز هم اشتباه کرد
با مرتبط کردن انرژی الکترون آزاد شده به زاویهی بین تابش الکترون و محور مولکول دو اتمی در تعداد زیادی برخورد فوتون-مولکول، پژوهشگران به طور الکترونیکی «طرح تداخلی» را باز تولید کردند. با نگاه کردن به جابجایی داپلریِ یون پس زده شده، محققان همچنین توانستند با محاسبه نشان دهند که آیا یک یا هر دو اتم پس زده می شوند. وقتی دو اتم با تداخل زیاد غیر قابل تشخیص بودند، نوارهای تداخلی ایجاد می شدند (شکل را ببینید). در حالی که وقتی به وضوح معلوم بود که تابش از کدام اتم آمده است، باند پیوسته ای به وجود میآمد که اثری از نوارهای تداخلی در آن دیده نمیشد. نتایج با تقریب خوبی با محاسبات سطح بالای نظری در توافق است- و بار دیگر نشان میدهد که تعبیر درست از آزمایش فرضی متعلق به بور است.

نظریه و آزمایش: الکترون آگر در عمل
جورج اشمیدمایر این کار را «نمایش زیبایی از یک اثر بسیار بنیادی» مینامد و توضیح میدهد که با اینکه در اصل «فیزیکِ آزمایش هاروچ و آزمایش ما دقیقاً یکی است اما تاکنون در سایر مقالات، شکاف، فوتون یا چیزی شبیه به آن بوده است. در اینجا شما دو ذره از ماده دارید که دو شکافیت را تشکیل میدهند. اینها گامهایی است که ما را به پیشنهاد اصلی اینشتین و بور نزدیک و نزدیکتر میکند». این تحقیق در Nature Photonics توضیح داده شده است.
در سال ۲۰۰۲، خوانندگانِ Physics World به آزمایش دو شکافی با الکترونها به عنوان «زیباترین آزمایش» رای دادند.
*سینکروترون ( synchrotron) که اولین بار توسط لوییس آلوارز ابداع شد، نوعی از شتاب دهنده ذرات به شکل یک حلقه دایرهیی است که با کمک میدان های الکتریکی و مغناطیسی، تابش الکترومغناطیسی تولید می کند ذراتی که با سرعتی نزدیک به سرعت نور در یک محیط الکترومغناطیسی حرکت میکنند، در جهت حرکتشان، نوری منتشر میکنند که تابش سینکروترون یا نور سینکروترون نامیده میشود.
ترجمه: مریم ذوقی
bigbangpage.com
منبع:انمن فیزیک هوپا
![[تصویر: 13910618000738_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000738_PhotoA.jpg)
![[تصویر: 13910618000744_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000744_PhotoA.jpg)
[/font]
![[تصویر: 13910618000750_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000750_PhotoA.jpg)
![[تصویر: 13910618000741_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000741_PhotoA.jpg)
![[تصویر: 13910618000742_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000742_PhotoA.jpg)
![[تصویر: 13910618000740_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000740_PhotoA.jpg)
![[تصویر: 13910618000743_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000743_PhotoA.jpg)
![[تصویر: 13910618000747_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000747_PhotoA.jpg)
![[تصویر: 13910618000748_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000748_PhotoA.jpg)
![[تصویر: 13910618000751_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000751_PhotoA.jpg)
[/b]
![[تصویر: 13910618000745_PhotoA.jpg]](http://media.farsnews.com/media/Uploaded/Files/Images/1391/06/18/13910618000745_PhotoA.jpg)
مسئله دیگری که از این هم جدیتر است، از کار افتادن دستگاههای NMR است. این دستگاهها اکثرا ساخت کشور آلمان بوده و هر سال باید توسط نمایندگی مجاز آن سرویس شوند. اما اکنون تحریم اتحادیه اروپا مانع از انجام این کار شده و دستگاههای NMR در تمام دانشگاههای ایران یکی پس از دیگری در حال از کار افتادن هستند. بدون این دستگاهها انجام تحقیقات پژوهشی و نوشتن مقالات علمی در زمینهی شیمی آلی تقریباً غیر ممکن است. با اینکه ارزش هر کدام از این دستگاهها بالغ بر 2 میلیارد تومان است ولی عملاً دیگر هیچ استفادهای برای پژوهشگران کشور ندارند. با توجه به اینکه اکنون دستگاههای NMR انگشت شماری در کشور فعالند، دانشجویان کارشناسی ارشد و دکترا برای تکمیل پایان نامههای خود مجبورند ماهها در نوبت گرفتن یک طیف NMRبایستند، آن هم با هزینههایی گزاف. این در حالی است که تا 5 سال پیش این کار در عرض چند دقیقه و به طور رایگان انجام میشد.